TRAITEMENT FŒTAL DE L’INFECTION CONGÉNITALE À CYTOMÉGALOVIRUS : ÉVALUATION DES NOUVEAUX ANTIVIRAUX, LE LETERMOVIR ET LE MERIBAVIR, ET ÉTUDE DE LEURS PASSAGES TRANSPLACENTAIRES DANS LE MODÈLE DE COTYLÉDON PERFUSÉ.
L’infection congénitale à cytomégalovirus (CMV) peut entrainer des séquelles sévères chez les foetus, nouveau-né et enfant (retard de développement, surdité). Lorsque la transmission verticale est confirmée, nous pensons que, débuter rapidement un traitement chez le foetus, pourrait améliorer son pronostic. Actuellement, le seul moyen est de donner le médicament à la mère dans le but de traiter le foetus. Ainsi, l’antiviral doit répondre à trois conditions : 1) être le moins toxique pour la mère 2) et pour le foetus 3) être capable de traverser le placenta. L’objectif final est donc de trouver un traitement de l’infection congénitale à CMV qui répond à ces conditions. Ainsi, nous avons évalué deux nouveaux antiviraux, le Letermovir (LMV) et le Maribavir (MBV) et étudié leurs passages transplacentaires dans le modèle du cotylédon perfusé.
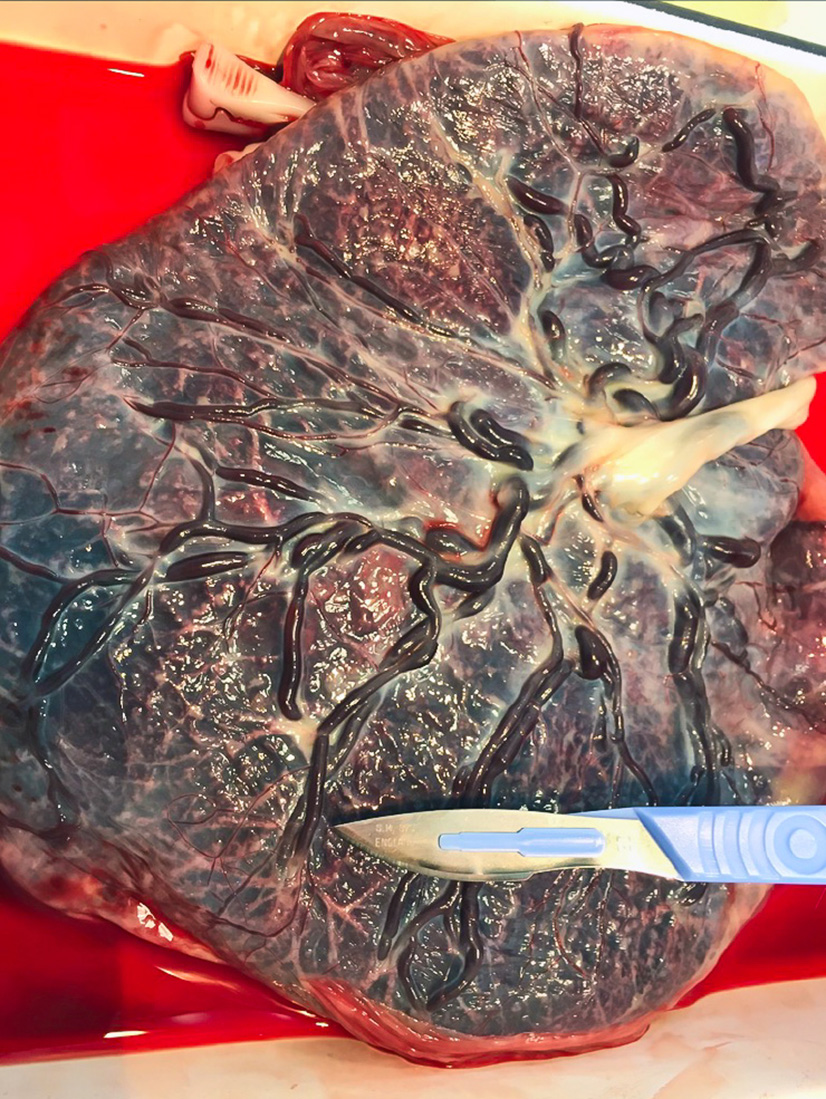
Nous avons étudié le passage transplacentaire de ces molécules dans le modèle du cotylédon perfusé, sur des placentas à terme, selon la méthode décrite par Schneider. La solution maternelle contenait : la drogue (LMV ou MBV) à une concentration cible égale à la concentration maximale utilisée en clinique, une solution de Earle, 2g/L d’albumine humaine, 20 g/L d’antipyrine (témoin de la viabilité du cotylédon). Les échantillons maternels et foetaux étaient prélevés toutes les 5 minutes pendant 90 minutes. Les concentrations étaient mesurées par chromatographie en phase liquide couplée à la spectrométrie de masse. Les paramètres suivants étaient mesurés : 1) les concentrations maternelle (CM) et foetale (CF) 2) le taux de transfert materno-foetal (TMF) : rapport entre la concentration foetale sur la concentration maternelle de l’antiviral 3) l’indice de Clairance (IC) : rapport entre le taux de transfert de la molécule sur celui de l’antipyrine. Un taux de TMF d’antipyrine Ñ 20% était nécessaire pour valider chaque expérience.
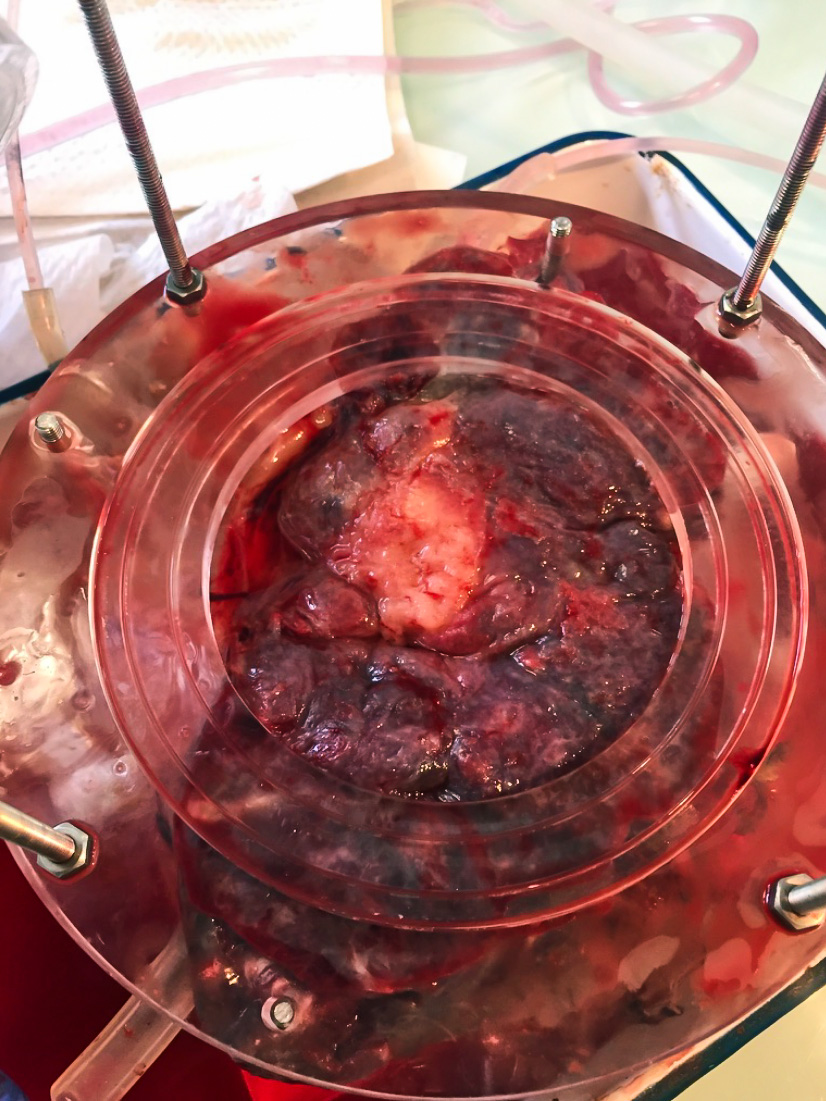
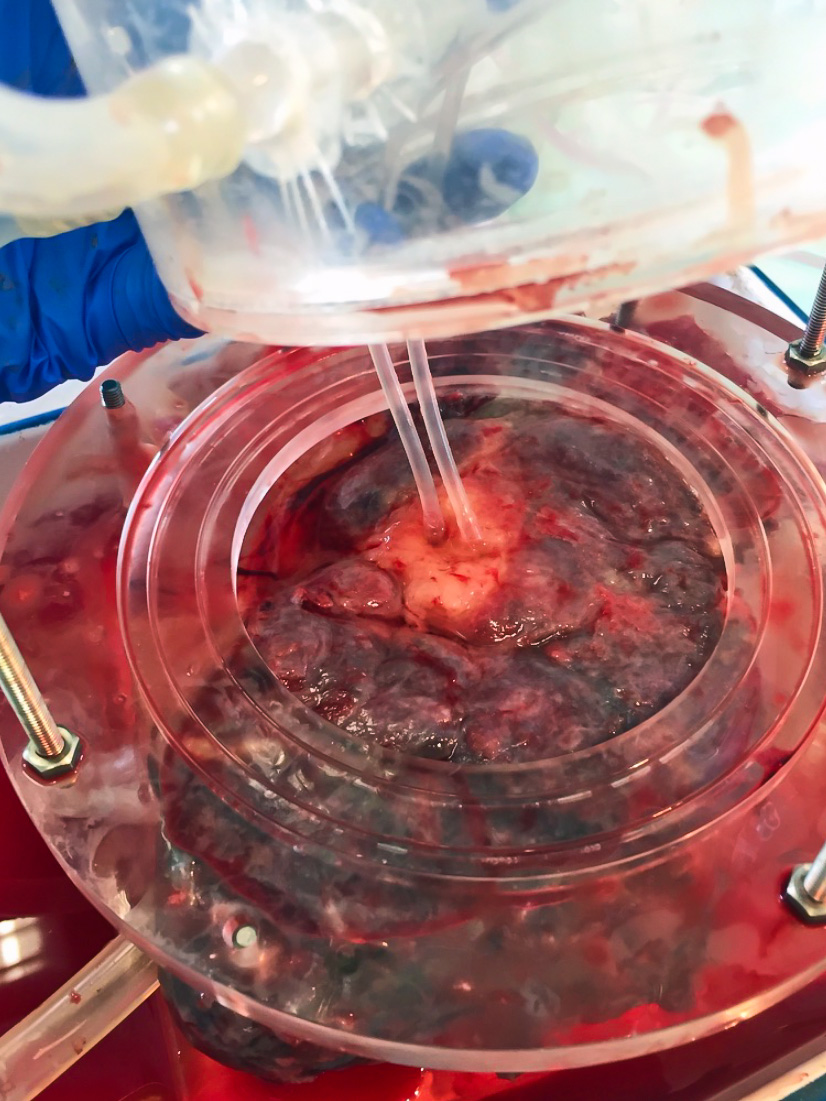
LA CHAÎNE DE PERFUSION PLACENTAIRE
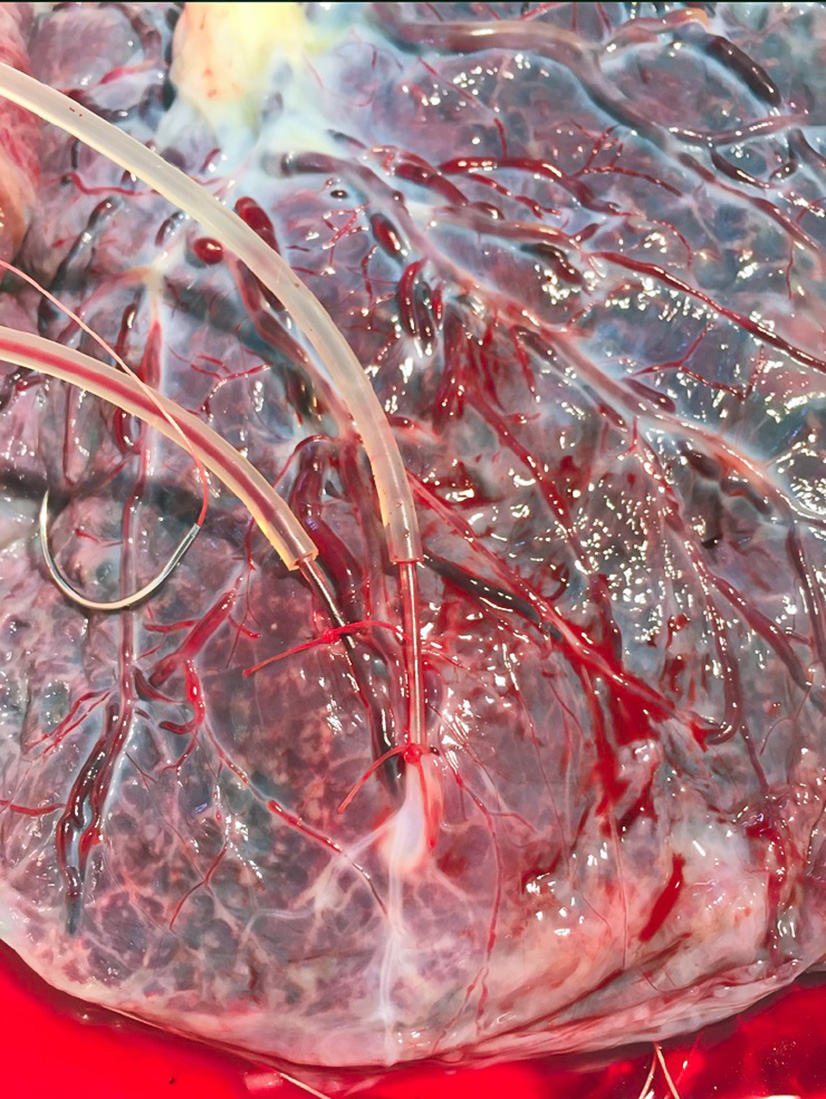
ÉTABLISSEMENT CIRCULATION MATERNO-FŒTALE
RÉSULTATS
LMV et MBV sont deux nouveaux antiviraux très efficaces contre le CMV. LMV, contrairement au MBV, a reçu l’agrément en 2017. Le profil de tolérance du LMV semble acceptable pour la mère et le foetus. Pour MBV, des études supplémentaires sont nécessaires, notamment sur la tératogénicité. Concernant le passage transplacentaire des molécules. Pour LMV : 5/10 placentas ont été validés avec un taux d’antipyrine moyen de 30 ± 12%. A l’état d’équilibre (entre T 30 min et T 90 min) : CF moyenne= 1,2 ± 0,5 mg/L , TMF moyen = 10 ± 5%, ICmoyen = 40 ± 23 %. Pour MBV : 3/8 placentas ont été validés avec un taux d’antipyrine moyen de 21 ± 3 %. A l’état d’équilibre (entre T20 min et T75 min) , CF moyenne=1,4 ± 0,3mg/L , TMF moyen =10 ± 2%, ICmoyen = 50 ± 7%.
CONCLUSION
LMV et MBV ont traversé la barrière placentaire à un taux bas à modéré ce qui est compatible avec leurs propriétés physico-chimiques. Leurs concentrations dans le compartiment foetal seraient efficaces pour traiter le foetus puisque les CF moyennes étaient supérieures aux concentrations moyennes inhibitrices des drogues (IC50%). La toxicité foetale du LMV serait moindre avec un profil de tolérance maternel acceptable. Le MBV est encore à l’état d’étude. Devant ces résultats encourageants, nous avons décidé de mettre en place un essai randomisé comparant l’efficacité virologique du LMV à celle du Valaciclovir chez des patientes porteuses d’un foetus infecté par le CMV.
MRI 3D MODELING OF A SURGICAL SCENE BEFORE FETOSCOPIC SURGERY
POURQUOI ?
Essor de la chirurgie fœtoscopique pour la prise en charge des malformations anténatales curables. Exemples : hernie de coupole diaphragmatique, VUP, STT …
Microchirurgie particulièrement compliquée du fait de la grossesse et des conditions opératoires variables : position placentaire, insertion ombilicale
Place de la chirurgie guidée par l’imagerie et des modélisations 3D
OBJECTIF
Réaliser un modèle 3D du pelvis féminin, de l’utérus et du placenta en per partum
Support : images IRM
En préopératoire d’une chirurgie fœtoscopique
MATÉRIELS & METHODES :
Trois femmes enceintes de grossesses simples
Au 3ème trimestre de la grossesse
Dont les fœtus ont des malformations diverses : atrésie digestive, malformation cardiaque, hernie de coupole diaphragmatique
Nécessitant la réalisation d’une IRM fœtale dans le cadre d’un bilan d’extension
IRM 1,5 Tesla, Séquences Fiesta (durée : 1min35)
Données IRM transférées sur le logiciel Slicer 3D version 4.8.1
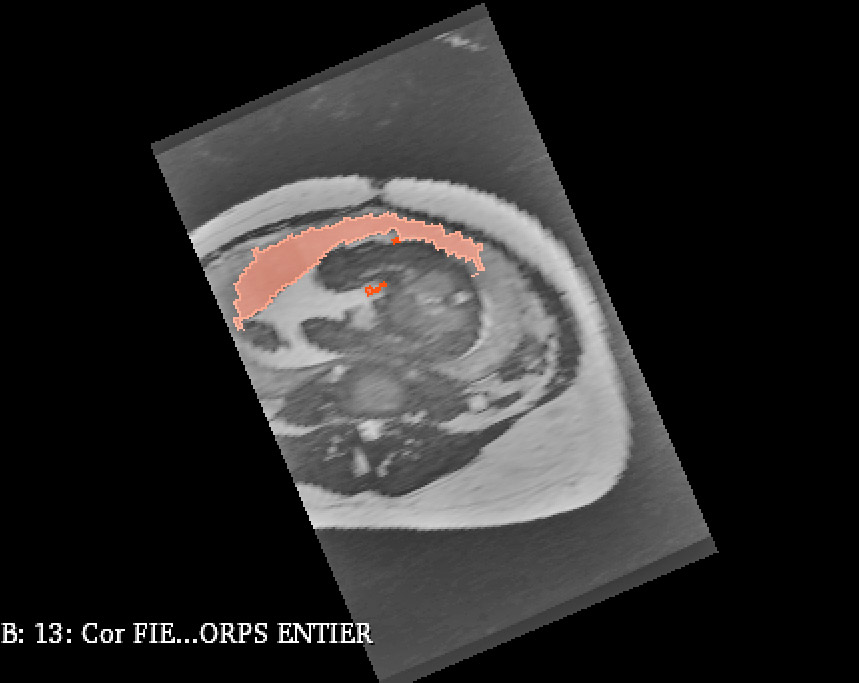
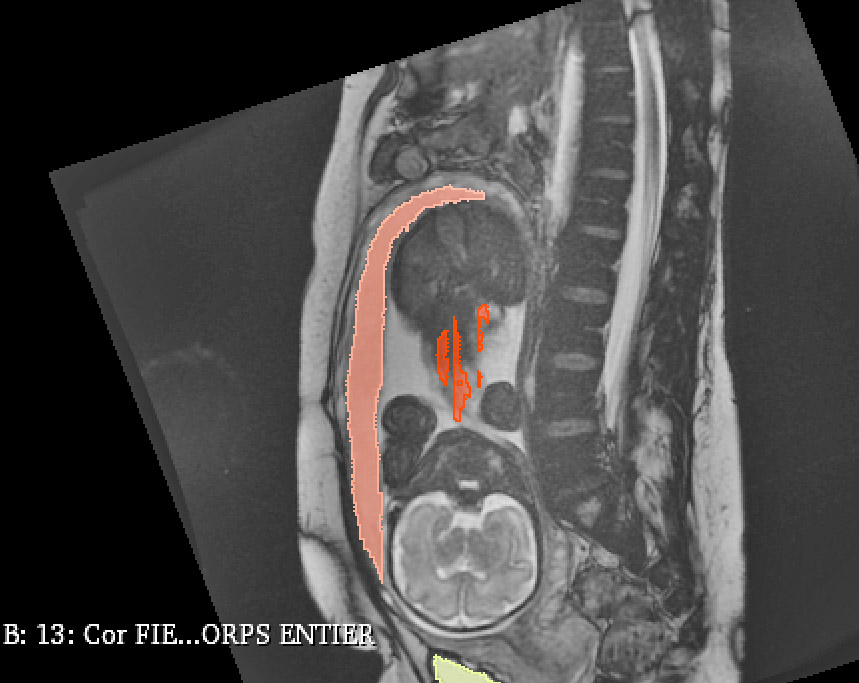
PRINCIPE DE SEGMENTATION
Segmentation en contourant et coloriant chaque structure anatomique
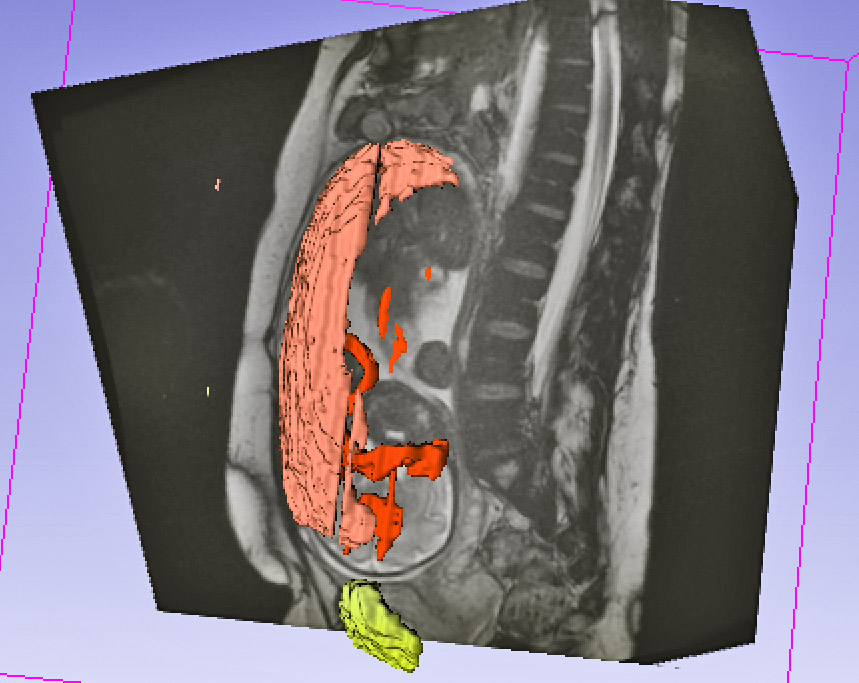
PREMIERS RÉSULTATS :
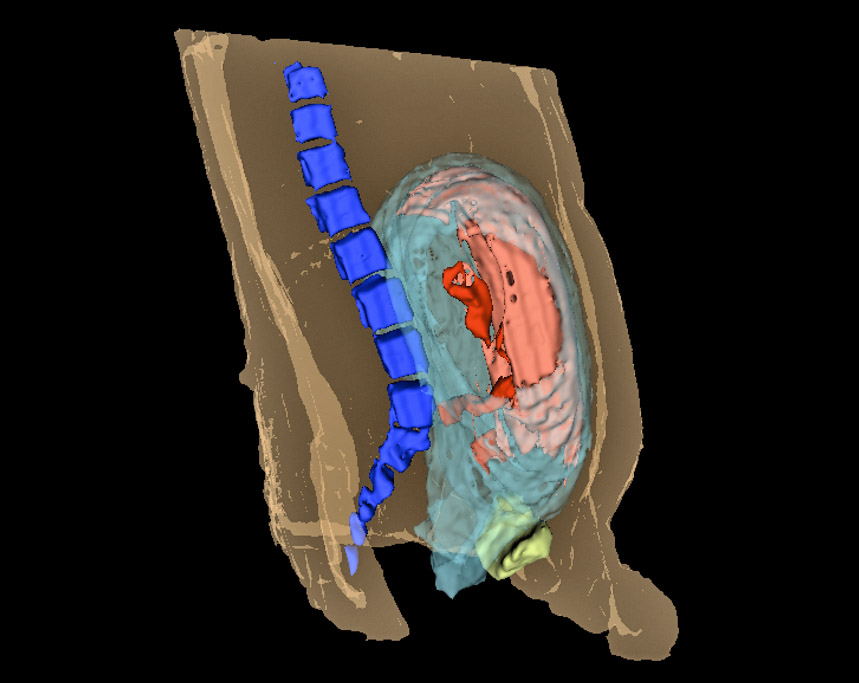
Modèle 3D d’un pelvis féminin durant la grossesse : utérus, placenta, cordon ombilical, colonne vertébrale et vessie maternelles
Manquent les os illiaques
Durée de la segmentation : 10-15 jours
Nécessité d’obtenir une fenêtre plus large d’acquisition en IRM
Nécessité d’une maîtrise du logiciel pour réduire au maximum le temps de segmentation
AVANCÉES
Segmentation initiale : utilisation des fonctions « paint » et « draw »
Contourage et coloriage de chaque structure anatomique
Possibilité de segmentation en une journée :
– Utilisation de la fonction « growing seeds »
– Automatisation de la segmentation
– Puis correction manuelle
DIFFICULTÉS RENCONTRÉES
Impossibilité d’obtenir une séquence cube (séquence isotropique) car repliement du fait des mouvements actifs fœtaux
Difficultés d’élargissement de la fenêtre d’acquisition
Conséquences :
– Segmentation moins précise
– Impossibilité de segmenter les petites structures anatomiques : uretères, artères utérines
CONCLUSION
Utilisation possible de l’IRM comme point de départ pour la modélisation 3D
Reproductibilité de la modélisation
Réduction du temps de segmentation
Obtention de séquences cubes ?
Développement d’algorithmes ?
INFECTIONS CONGÉNITALES À CYTOMÉGALOVIRUS
L’équipe de l’unité PACT (Prise en charge de anomalies congénitales et leur traitement) au sein de l’hôpital Necker Enfants Malades avec le Centre National de Référence (CNR) virologique sur le CMV, présente la plus grande expertise multidisciplinaire sur ce sujet et relève tous les défis posées par cette infection avant la naissance.
Nous avons développé une expertise particulière dans l’évaluation du risque d’infection fœtale chez les femmes présentant une première infection en début de grossesse.
Le premier volet de l’étude CYMEPEDIA a permis de préciser la prévalence et la sociologie de l’infection congénitale à CMV à la naissance en Ile-de-France, soit 0,37% des naissances.
- Notre laboratoire a développé une expertise particulière dans l’isolement du virus dans un simple écouvillon salivaire ou sur une goutte de sang séchée sur un buvard
- La moitié de ces infections sont la conséquence de la transmission d’ une première infection de la femme enceinte
- L’autre moitié survient chez les enfants de femmes déjà immunisées
- La gravité est la même dans ces deux populations d’enfants puisque XX% ont des symptômes à la naissance de même nature dans les deux cas.
- La typologie des populations exposées est bien définie : Pour les primo-infections, il s’agit de femmes jeunes d’un environnement socio-économique favorisé dont la contamination se fait par leur premier enfant en âge pré-scolaire, en particulier en crèche. Les infections non-primaires touches des femmes jeunes qui sont souvent issues de l’immigration sont exposées à travers une communauté d’enfants, leur niveau socio-économique est souvent bas et le chômage plus fréquent.
Le deuxième volet de l’étude CYMEPEDIA qui permet d’observer le devenir des enfants infectés a d’ores et déjà permis d’affirmer que la période critique de l’infection maternelle pour le risque du développement de l’enfant était le premier trimestre de la grossesse.
L’étude CYMEVAL a permis de préciser le pronostic et les risques d’anomalies du développement en fonction des symptômes présentés in utero par les fœtus infectés. Les principaux déterminants en sont le terme à l’infection maternelle, les signes échographiques, la quantité de virus circulant dans le sang fœtal et le retentissement sur la production des plaquettes s-du sang fœtal.
L’étude CYMEVAL a montré qu’il était possible de diminuer les symptômes de l’infection à la naissance des fœtus infectés symptomatiques en administrant un traitement antiviral à la femme enceinte
Les défis que nous souhaitons relever sont bien définis et les moyens nécessaires pour y parvenir sont connus et chiffrés.
1/ Il n’existe aujourd’hui aucun moyen de faire le diagnostic d’une infection non primaire à CMV chez une femme enceinte.
La sérologie (IgG, IgM, avidité des IgG si IgM positives) permet le diagnostic de primo-infection pendant la grossesse. Il n’y a pas de méthode validée pour diagnostiquer une infection maternelle secondaire. Le diagnostic de l’infection fœtale se fait par PCR dans le liquide amniotique et est indiqué en cas de symptômes fœtaux évocateurs ou de primo-infection maternelle. Lors d’une infection le virus persiste dans les urines jusqu’à 250 jours et 4% des femmes enceintes déjà immunisées ont du virus dans leur urines au 1er trimestre.
Nous souhaitons étudier la possibilité d’une infection secondaire chez 2000 femmes immunisées avant la grossesse et en recueillir le devenir. Ce diagnostic sera fait par une amplification du génome viral par PCR dans les urines de ces femmes au premier trimestre.
Coût de l’étude : 130 000 euros sur 18 mois
Z
2/ La part individuelle génétique de la susceptibilité à développer une infection congénitale grave est très vraisemblable mais inconnue à ce jour
De nombreuses études de différents groupes, dont le nôtre, n’ont pas permis de retrouver un lien entre le génotype de la souche, défini par la séquence de certains gènes codant pour des protéines jouant un rôle important dans la physiopathologie de l’infection, et la sévérité de l’infection congénitale. Nous allons tester rétrospectivement le génome de fœtus et de nouveau-nés infectés par le cmv en fonction de la gravité des lésions développées.
Pour ce faire une étude de l’exome sera réalisée dans 20 cas présentant des séquelles sévères et comparé à 20 cas ne présentant pas de séquelle selon la définition de l’étude. Nous étudierons également les gènes de l’immunité dans l’ensemble des individus de la cohorte quel que soit le statut clinique : absence de séquelle, séquelle minimes, séquelles modérées ou séquelles sévères.
Coût de l’étude : 15 000 euros
ÉTUDE FINANCEE EN COURS
Z
3/ Une thérapie prénatale efficace pour les fœtus infectés à haut risque de lésions cérébrales est nécessaire
Le pronostic de l’infection fœtale peut être établi lors d’une imagerie fœtale (échographie (US) / IRM) combinée à des tests de laboratoire (1). Le pronostic est mauvais pour les lésions cérébrales sévères et bon avec des paramètres d’imagerie et de laboratoire normaux. Dans l’intervalle, les fœtus symptomatiques présentant des caractéristiques cérébrales extra-cérébrales ou bénignes constituent une cible appropriée pour le traitement antiviral afin de prévenir le développement de lésions cérébrales irréversibles.
Le valaciclovir (VACV), bien toléré pendant la grossesse, a été administré à des femmes portant un fœtus présentant au moins un signe échographique d’infection qui a conduit 79% des nouveau-nés traités à naître asymptomatiques par rapport à 43% après l’histoire naturelle de la maladie.
Seuls 57% des fœtus avec plus de 1 symptôme prénatal sont nés asymptomatiques, ce qui suggère une baisse de l’efficacité du VACV dans de tels cas. De plus, bien que la charge virale du sang fœtal ait diminué avec le traitement, 90% des fœtus traités présentaient toujours un ADN du CMV détectable dans le sang de cordon à la naissance.
Le letermovir (LET, disponible en 2018) a une nouvelle activité anti-CMV spécifique et, dans les études de toxicité préclinique, a été bien toléré, non génotoxique ni tératogène et n’a pas altéré la fertilité à la dose recommandée chez l’humain (5). En outre, aucune préoccupation spécifique ne découle de son profil de sécurité chez l’homme (5). Il contrôle l’infection à CMV et la maladie chez les patients ayant subi une greffe de moelle osseuse en réalisant une clairance de la charge virale dans 50 à 80% des cas (3,4). Nous émettons l’hypothèse que le traitement maternel avec LET inhibera la réplication du CMV fœtal mieux que le VACV chez les fœtus infectés symptomatiques et conduira à une proportion plus élevée de PCR CMV négative à la naissance dans le sang de cordon ombilical.
Nous proposons de comparer le VACV au léterrmovir dans un essai randomisé
Coût de l’étude : 500 000 euros
DEMANDE DE FINANCEMENT EN COURS AU PHRC 2018
Z
4/ Il n’existe pas de prévention efficace de la transmission materno-fœtale lors d’une primo-infection maternelle au premier trimestre de la grossesse.
Le dépistage universel de la primo-infection maternelle et celui de l’infection néonatale ne sont pas recommandés à ce jour principalement en raison de l’absence de prévention efficace de la transmission du virus au fœtus. Il n’y a pas de prophylaxie de l’infection congénitale à CMV: pas de vaccin, résultats contradictoires sur les mesures d’hygiène et sur les globulines hyperimmunes pour éviter la transmission verticale. L’inhibition précoce de la réplication virale par un traitement antiviral chez les femmes infectées en début de grossesse devrait limiter le taux de transmission materno-fœtale. Ce taux est en moyenne de 35% et nous faisons l’hypothèse qu’un traitement par Letermovir dès le diagnostic d’infection maternelle et pendant 8 semaines pourrait réduire la fréquence des infections fœtales vérifiée par amniocentèse de 50%.
Coût de l’étude : 250 000 euros
Z
5/ Étude du passage transplacentaire du Letermovir et du Maribavir sur modèle de cotylédon placentaire perfusé
Nous avons montré que ces nouveaux antiviraux particulièrement efficaces sur le CMV et peu toxiques présentaient tous les 2 un passage transplacentaire aboutissant à une concentration efficace dans le compartiment foetal
Coût de l’étude : 7 000 euros
ÉTUDE FINANCÉE ET RÉALISÉE
Z
ÉTUDES MENÉES PAR PACT SUR L’INFECTION CONGENITALE À CMV :
CYMEVAL (Financement PHRC 2012-2016): Traitement par le valaciclovir des foetus infectés et symptomatiques in utero
CYMEPEDIA (Financement PHRC 2012-2020) : Epidémiologie de l’infection congénitale en Ile-de-France et pronostic à 2 ans des enfants infectés
CYMEAUDIT (Financement PHRC 2012-2018) : Faisabilité du dépistage simultané de la surdité et de l’infection congénitale à CMV dans les premiers jours de vie.
BIOCMV (Financement CNR Herpes-Virus) : Banque de données déclarée à la CNIL, de liquide amniotique et de sérums de paires mère-enfant dans l’infection à CMV
Z
BIBLIOGRAPHIE PACT SUR L’INFECTION CONGENITALE A CMV
Leruez-Ville M, Magny JF, Couderc S, Pichon C, Parodi M, Bussières L, Guilleminot T, Ghout I, Ville Y. Risk Factors for Congenital Cytomegalovirus Infection Following Primary and Nonprimary Maternal Infection: A Prospective Neonatal Screening Study Using Polymerase Chain Reaction in Saliva. Clin Infect Dis. 2017 Aug 1;65(3):398-404.
Khalil A, Jones C, Ville Y. Congenital cytomegalovirus infection: management update.
Curr Opin Infect Dis. 2017 Jun;30(3):274-280.
Leruez-Ville M, Ghout I, Bussières L, Stirnemann J, Magny JF, Couderc S, Salomon LJ, Guilleminot T, Aegerter P, Benoist G, Winer N, Picone O, Jacquemard F, Ville Y. In utero treatment of congenital cytomegalovirus infection with valacyclovir in a multicenter, open-label, phase II study. Am J Obstet Gynecol. 2016 Oct;215(4):462.e1-462.e10
Reply.
Ville Y, Leruez-Ville M.
Am J Obstet Gynecol. 2017 Feb;216(2):197. doi: 10.1016/j.ajog.2016.09.094. Epub 2016 Sep 22. No abstract available.
Leruez-Ville M, Ville Y. Fetal cytomegalovirus infection. Best Pract Res Clin Obstet Gynaecol. 2017 Jan;38:97-107.
Bilavsky E, Pardo J, Attias J, Levy I, Magny JF, Ville Y, Leruez-Ville M, Amir J. Clinical Implications for Children Born With Congenital Cytomegalovirus Infection Following a Negative Amniocentesis. Clin Infect Dis. 2016 Jul 1;63(1):33-8.
Desveaux C, Klein J, Leruez-Ville M, Ramirez-Torres A, Lacroix C, Breuil B, Froment C, Bascands JL, Schanstra JP, Ville Y. Identification of Symptomatic Fetuses Infected with Cytomegalovirus Using Amniotic Fluid Peptide Biomarkers. PLoS Pathog. 2016 Jan 25;12(1):e1005395.
Leruez-Ville M, Ville Y. Optimum treatment of congenital cytomegalovirus infection.
Expert Rev Anti Infect Ther. 2016;14(5):479-88.
Sellier Y, Guilleminot T, Ville Y, Leruez-Ville M. Comparison of the LIAISON(®) CMV IgG Avidity II and the VIDAS(®) CMV IgG Avidity II assays for the diagnosis of primary infection in pregnant women. J Clin Virol. 2015 Nov;72:46-8.
Ville Y, Leruez-Ville M. Managing infections in pregnancy. Curr Opin Infect Dis. 2014 Jun;27(3):251-7.
Leruez-Ville M, Sellier Y, Salomon LJ, Stirnemann JJ, Jacquemard F, Ville Y. Prediction of fetal infection in cases with cytomegalovirus immunoglobulin M in the first trimester of pregnancy: a retrospective cohort. Clin Infect Dis. 2013 May;56(10):1428-35.
Avettand-Fenoel V, Magny JF, Ville Y, Leruez-Ville M. Virological tools for the diagnosis, the prognosis and the surveillance of congenital cytomegalovirus infections]. Arch Pediatr. 2013 Feb;20(2):204-8.
Benoist G, Leruez-Ville M, Magny JF, Jacquemard F, Salomon LJ, Ville Y. Management of pregnancies with confirmed cytomegalovirus fetal infection. Fetal Diagn Ther. 2013;33(4):203-14. doi: 10.1159/000342752.
Leruez-Ville M, Vauloup-Fellous C, Couderc S, Parat S, Castel C, Avettand-Fenoel V, Guilleminot T, Grangeot-Keros L, Ville Y, Grabar S, Magny JF. Prospective identification of congenital cytomegalovirus infection in newborns using real-time polymerase chain reaction assays in dried blood spots. Clin Infect Dis. 2011 Mar 1;52(5):575-81
Coll O, Benoist G, Ville Y, Weisman LE, Botet F, Anceschi MM, Greenough A, Gibbs RS, Carbonell-Estrany X; WAPM Perinatal Infections Working Group. Guidelines on CMV congenital infection. J Perinat Med. 2009;37(5):433-45
Benoist G, Salomon LJ, Mohlo M, Suarez B, Jacquemard F, Ville Y. Cytomegalovirus-related fetal brain lesions: comparison between targeted ultrasound examination and magnetic resonance imaging. Ultrasound Obstet Gynecol. 2008 Dec;32(7):900-5.
Benoist G, Salomon LJ, Jacquemard F, Daffos F, Ville Y. The prognostic value of ultrasound abnormalities and biological parameters in blood of fetuses infected with cytomegalovirus.
BJOG. 2008 Jun;115(7):823-9.
Benoist G, Jacquemard F, Leruez-Ville M, Ville Y. Cytomegalovirus (CMV) congenital infection]. Gynecol Obstet Fertil. 2008 Mar;36(3):248-60.
Picone O, Costa JM, Chaix ML, Ville Y, Rouzioux C, Leruez-Ville M. Comments on “cytomegalovirus (CMV)-encoded UL144 (truncated tumor necrosis factor receptor) and outcome of congenital CMV infection”. J Infect Dis. 2007 Dec 1;196(11):1719-20.
Jacquemard F, Yamamoto M, Costa JM, Romand S, Jaqz-Aigrain E, Dejean A, Daffos F, Ville Y. Maternal administration of valaciclovir in symptomatic intrauterine cytomegalovirus infection. BJOG. 2007 Sep;114(9):1113-21. Epub 2007 Jul 6.
Picone O, Costa JM, Dejean A, Ville Y. Is fetal gender a risk factor for severe congenital cytomegalovirus infection? Prenat Diagn. 2005 Jan;25(1):34-8.